ЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈ,вВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈ
ВЉЮФбЇЯАЭјаЁБрЮЊФњЪеМЏећРэЕФЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈ,вВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈ,ЬсЙЉШЋУцЕФЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈ,вВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈаХЯЂ,ЯЃЭћЖдФњгагУ!
ЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈ,вВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈЦЊвЛЃК2012ЛЏбЇзЈЬтИДЯА1
2012ЛЏбЇзЈЬтИДЯА
ЯжгаШчЯТвЧЦїЃК
гУвЧЦїУћГЦЛиД№ЃК
ЃЈ1ЃЉПЩвджБНгМгШШЕФвЧЦїЪЧ ЪдЙм
ЃЈ2ЃЉгУгкЮќШЁКЭЕЮМгЩйСПвКЬхЕФЪЧ
НКЭЗЕЮЙм
ЃЈ3ЃЉгУгкНЯДѓСПвКЬхЕФЗДгІШнЦїЪЧ ЩеБ
ЃЈ4ЃЉЪеМЏКЭДЂДцЩйСПЦјЬхЕФЪЧМЏЦјЦП
ЃЈ5ЃЉПЩвдЦ№ЙЬЖЈжЇГХзїгУЕФвЧЦїЪЧЬњМмЬЈ
ЃЈ6ЃЉПЩвдгУгкзЊвЦЁЂв§СїЕФвЧЦїЪЧ ВЃСЇАє
ЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈЃЌвВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈЃЎ
ЃЈ1ЃЉЮвУЧвбОбЇЙ§ЪЕбщЪвжЦШЁбѕЦјКЭЖўбѕЛЏЬМСНжжЦјЬхЕФЗДгІдРэЁЂжЦШЁгыЪеМЏЗНЗЈЃЎЧыФуЙщФЩГіЪЕбщЪвжЦШЁЦјЬхЗДгІЕФЙВЭЌЕуЃК ЂлЂн
ЃЈЬюађКХЃЉЃЎ
ЂйашвЊМгШШ ЂкЪЙгУДпЛЏМС ЂлУЛгаЦјЬхВЮМгЗДгІ ЂмдСЯЮЊДПОЛЮя ЂнжЛЩњГЩвЛжжЦјЬх
ЃЈ2ЃЉбЁдёжЦШЁЦјЬхЕФЗЂЩњзАжУЪБвЊПМТЧ ЗДгІЮяЕФзДЬЌКЭЗДгІЬѕМўЃЌЖјбЁдёЪеМЏЦјЬхЕФзАжУгІПМТЧ ЦјЬхдкЫЎжаЕФШмНтадвдМАЦјЬхУмЖШЕФДѓаЁЃЌФмЗёгыПеЦјЗДгІЃЌФмЗёгыЫЎЗДгІ
ЃЈ3ЃЉНсКЯЭМЪОЪЕбщзАжУЃЌЛиД№ЯТСаЮЪЬтЃЎ
ЯжгаЯТСаЮяжЪЃКЂйЧтЦјЁЂЂкЕЊЦјЁЂЂлКЄЦјЁЂЂмУїЗЏЁЂЂнбѕЦјЁЂЂоЫЎЃЌИљОнЫљбЇЕФжЊЪЖЃЌАДвЊЧѓЬюПеЃЈЬюађКХЃЉЃК
ЃЈ1ЃЉОпгаПЩШМадЕФЦјЬхЪЧ Ђй
ЃЈ2ЃЉПЩДњЬцЧтЦјзіЬНПеЦјЧђЕФЯЁгаЦјЬхЂл
ЃЈ3ЃЉГЃгУгкОЛЫЎЕФЮяжЪЪЧЂм
ЃЈ4ЃЉШЫЬхФкКЌСПзюЖрЕФЛЏКЯЮяЪЧЂо
ЂйаДГіДјБъКХвЧЦїЕФУћГЦЃКa ОЦОЋЕЦЃЌb ГЄОБТЉЖЗ
ЂкаЁЗНЭЌбЇгУAзАжУжЦШЁбѕЦјЃЌЗДгІЕФЗћКХБэДяЪНЮЊ
KMnO4 =K2MnO4+MnO2+O2ЁќЃЌЃЎзАжУжаУоЛЈЭХЕФзїгУЪЧЗРжЙМгШШЪБИпУЬЫсМиЗлФЉНјШыЕМЙмЖјгАЯьЦјЬхЕМГіЃЎ
ЂлаЁЭѕЭЌбЇШЯЮЊгУBзАжУвВПЩжЦШЁбѕЦјЃЌЕЋвЊПМТЧПижЦЗДгІЕФЫйТЪЃЌвђДЫгІИУАбBзАжУжаЕФbвЧЦїЛЛГЩ ЗжвКТЉЖЗЃЈЬювЛжжвЧЦїУћГЦЃЉЃЎ
ЂмаЁУїЭЌбЇБОЯыгУBзАжУжЦШЁЖўбѕЛЏЬМЃЌЕЋаЁУїАЎЖЏЪжзіЪЕбщЃЌЫћевРДвЛаЉЫмСЯЦПКЭЦфЫћгУЦЗЃЌжЦГЩШчЭМDЫљЪОЕФзАжУЃЎИУЗДгІЕФЗћКХБэДяЪНЪЧ HCl+CaCO3=CaCl2+H2O+CO2ЁќЃЌИУзАжУзїЮЊжЦШЁЖўбѕЛЏЬМЦјЬхЗЂЩњзАжУЕФгХЕуЪЧПЩвдЫцвтПижЦЗДгІЕФЗЂЩњКЭЭЃжЙ
ЃЈ4ЃЉЪЕбщЙ§ГЬжавЊНјаавЉЦЗШЁгУЁЂЮяжЪМгШШЁЂвЧЦїЯДЕгЕШЛљБОВйзїЃЌЦфжаЭљЭљЩцМАгУСПЮЪЬтЃЎЯТСаЙигкгУСПЕФЫЕЗЈВЛе§ШЗЕФЪЧ BC
ЃЈЬюађКХЃЉЃЎ
AЃЎИјЪдЙмРяЕФвКЬхМгШШЪБЃЌвКЬхВЛГЌЙ§ЪдЙмШнЛ§ЕФ1/3
BЃЎИјЩеБФкЕФвКЬхМгШШЪБЃЌвКЬхСПВЛГЌЙ§ЩеБШнЛ§ЕФ1/3
CЃЎШЁгУвКЬхЪБЃЌШчЙћУЛгаЫЕУїгУСПЃЌвКЬхвЛАуШЁ5mL
DЃЎЪЙгУОЦОЋЕЦЪБЃЌОЦОЋЕЦФкЕФОЦОЋВЛГЌЙ§ОЦОЋЕЦШнЛ§ЕФ2/3
ЃЈ5ЃЉЭЈЙ§ВщдФзЪСЯЕУжЊЃКАБЦјЃЈNH3ЃЉЪЧвЛжжУмЖШБШПеЦјаЁЧвМЋвзШмгкЫЎЕФЦјЬхЃЌЦфЫЎШмвКГЦЮЊАБЫЎЃЛаЁЗМЭЌбЇМгШШТШЛЏяЇКЭЧтбѕЛЏИЦЕФЙЬЬхЛьКЯЮяжЦШЁАБЦјЃЌЫ§гІбЁдёЕФЗДгІЗЂЩњзАжУЪЧA
ЃЈЬюзжФИЃЉЃЌЪеМЏАБЦјЪБЃЌгІДгCзАжУЕФ dЃЈЬюЁАcЁБЛђЁАdЁБЃЉЙмПкЭЈШыЃЎ
11ЁЂЃЈ2010?ФЯФўЃЉЧыФугУвбОеЦЮеЕФЪЕбщЪвгаЙиЦјЬхжЦШЁКЭОЛЛЏЕШжЊЪЖЛиД№ЯТСаЮЪЬтЃКЃЈ1ЃЉаДГіЩЯЭМжаaЁЂbвЧЦїУћГЦЃКa ОЦОЋЕЦ bЫЎВл
ЃЈ2ЃЉЪЕбщЪвгУИпУЬЫсМижЦШЁбѕЦјЪБЃЌПЩбЁгУЕФЗЂЩњзАжУЪЧ B
ЃЈЬюзАжУДњКХЃЉЃЌCзАжУЪеМЏбѕЦјЃЌШчКЮШЗЖЈЦјЬхвбОЪеМЏТњгУДјЛ№аЧЕФФОЬѕЗХЕНМЏЦјЦППкЃЌШчЙћФОЬѕИДШМОЭЫЕУївбОЪеМЏТњЃЌЪЕбщНсЪјЪБЕФе§ШЗВйзїЫГађЮЊЃКЯШвЦГіЕМЦјЙмКѓЭЃжЙМгШШЃЌаДГіИУЗДгІЕФЛЏбЇЗНГЬЪНЃК 2KMnO4 = K2MnO4+MnO2+O2Ёќ
ЃЈ3ЃЉШєгУFзАжУЪеМЏO2ЃЌдђO2гІДгЕМЙмПкcЃЈЬюЁАcЁБЛђЁАdЁБЃЉЭЈШыЃЎ
ЃЈ4ЃЉШєгУEзАжУЪеМЏФГжжЦјЬхЃЌдђИУжжЦјЬхгІОпБИЕФаджЪЪЧУмЖШБШПеЦјаЁ ЃЌЪдаДГівЛИіжЦШЁИУжжЦјЬхЕФЛЏбЇЗНГЬЪНЃК 2HCl+Zn=ZnCl2+H2Ёќ
ЃЈ5ЃЉФГПЮЭтаЁзщЕФЭЌбЇгУЩЯЭМBзАжУЪЙВнЫсЗжНтВЂгУШчЯТзАжУЬНОПВнЫсЗжНтЕФВњЮяЃК
ЙХЪЋДЪЪЧЧАШЫИјЮвУЧСєЯТЕФБІЙѓВЦИЛЃЎЯТСаЪЋОфжажЛЩцМАЮяРэБфЛЏЕФЪЧЃЈ ЃЉ
AЁЂжЛвЊЙІЗђЩюЃЌЬњшЦФЅГЩеыBЁЂвАЛ№ЩеВЛОЁЃЌДКЗчДЕгжЩњ
CЁЂДКВЯЕНЫРЫПЗНОЁЃЌРЏОцГЩЛвРсЪМИЩ
DЁЂБЌжёЩљжавЛЫъГ§ЃЌДКЗчЫЭХЏ
7ЁЂЃЈ2009?ДѓСЌЃЉЯТСаСЃзгжаЃЌЪєгкЙЙГЩЮяжЪЕФЛљБОСЃзгЕФЪЧЃЈ ЃЉ
AЁЂжЪзг BЁЂжазг CЁЂЕчзг DЁЂдзг
8ЁЂЃЈ2003?ЮкТГФОЦыЃЉЯТСаЮяжЪжаЪєгкЛьКЯЮяЕФЪЧЃЈ ЃЉ
AЁЂЦЁОЦ BЁЂвКЬЌбѕЦј CЁЂЕЊЦј DЁЂЖўбѕЛЏЬМ
ЃЈ2004?ЗРГЧИлЃЉФГЯћЖОМСЕФгааЇГЩЗнЪЧДЮТШЫсФЦЃЈNaClOЃЉЃЌдкNaClOжаТШдЊЫиЕФЛЏКЯМлЪЧЃЈ ЃЉ
AЁЂ+1Мл BЁЂ-1Мл CЁЂ+3Мл DЁЂ+5Мл
1.гУЁАЮяРэБфЛЏЁЂЛЏбЇБфЛЏЁЂЮяРэаджЪЁЂЛЏбЇаджЪЁБЬюПеЃЎ
ЃЈ1ЃЉжВЮяНјааЙтКЯзїгУ ЛЏбЇБфЛЏ
ЃЈ2ЃЉЬњж§ГЩЙјЮяРэБфЛЏ
ЃЈ3ЃЉУОШМЩеФмЩњГЩбѕЛЏУОЛЏбЇаджЪ
ЃЈ4ЃЉБљбЉЯћШк ЮяРэБфЛЏ
ЃЈ5ЃЉУОЪЧвјАзЩЋЕФЙЬЬхЃЎЮяРэаджЪ
ЃЈ6ЃЉОЦОЋЛгЗЂЃЎЮяРэБфЛЏ
ЃЈ7ЃЉЪГЮяИЏРУ ЛЏбЇБфЛЏ
ЃЈ8ЃЉЭЫПЭфЧњ ЮяРэБфЛЏ
2. ЯТСаУшЪіжаЪєгкЮяРэБфЛЏЕФЪЧЂнЃЌЪєгкЛЏбЇБфЛЏЕФЪЧЂлЃЌЪєгкЮяРэаджЪЕФЪЧЂкЂмЃЌЪєгкЛЏбЇаджЪЕФЪЧ ЂйЃЎЂйЭТЬКЭЬМЙВШШЛсЩњГЩЭЃЛЂкДПОЛЕФЫЎЪЧЮоЩЋЮоЮЖЕФвКЬхЃЛЂлУОДјдкПеЦјжаШМЩеЃЛЂмбѕЦјВЛвзШмгкЫЎЧвУмЖШБШПеЦјДѓЃЛЂнФОАєЪмСІелЖЯЃЎ
.ЂйЬњШлЛЏГЩЬњЫЎЃЛЂкХДУзФ№ГЩОЦЃЛЂлЬњдкГБЪЊЕФПеЦјжаШнвзЩњатЃЛЂмЕЦХнжаЕФЮйЫПЭЈЕчКѓЗЂШШЗЂЙтЃЛЂнЪГЮяИЏРУЃЛЂоФОВёШМЩеЃЛЂпЕЈЗЏЪЧРЖЩЋЙЬЬхЃЎЩЯЪіМИжжЧщПіжаЃЈгУађКХЬюПеЃЉЃК
ЃЈ1ЃЉЪєгкУшЪіЮяРэаджЪЕФЪЧ ЂпЃЌУшЪіЛЏбЇаджЪЕФЪЧ Ђл
ЃЈ2ЃЉЪєгкЮяРэБфЛЏЕФЪЧ ЂйЂмЃЌЪєгкЛЏбЇБфЛЏЕФЪЧ ЂкЂнЂо
3. бЁгУЂйЮяРэБфЛЏ ЂкЛЏбЇБфЛЏ ЂлЮяРэаджЪ ЂмЛЏбЇаджЪЃЌЬюаДЯТСаПеАзЃЈгУађКХЃЉ
ЃЈ1ЃЉУКЦјШМЩе ЂкЃЈ2ЃЉЫЎЗаЬкБфГЩЫЎеєЦј ЂйЃЈ3ЃЉОЦОЋвзЛгЗЂ ЂлЃЈ4ЃЉЬњдкГБЪЊЕФПеЦјжавзЩњатЂм
4. бЁгУЂйЮяРэБфЛЏ ЂкЛЏбЇБфЛЏ ЂлЮяРэаджЪ ЂмЛЏбЇаджЪЃЌЬюаДЯТСаПеАзЃЈгУађКХЃЉ
ЃЈ1ЃЉУКЦјШМЩе ЂкЃЛЃЈ2ЃЉЫЎЗаЬкБфГЩЫЎеєЦјЂйЃЈ3ЃЉОЦОЋвзЛгЗЂЂл
ЃЈ4ЃЉЬњдкГБЪЊЕФПеЦјжавзЩњат
5ЩшМЦЪЕбщМјБ№ЯТСаЮяжЪЃЈВйзїЁЂЯжЯѓЁЂНсТлЃЉЃК
ЃЈ1ЃЉЫЎКЭОЦОЋ
РћгУЮяРэаджЪМјБ№ЃК ЗжБ№ШЁбљЦЗЮХЦјЮЖЃЌгаЗМЯуЮЖЕФЪЧОЦОЋЃЌУЛгаЮЖЕРЕФЪЧЫЎ РћгУЛЏбЇаджЪМјБ№ЃК ЗжБ№НЋбљЦЗЕуШМЃЌФмШМЩеЕФЕФЪЧОЦОЋЃЌВЛФмШМЩе
ЃЈ2ЃЉбѕЦјКЭЖўбѕЛЏЬМЃКРћгУЮяРэаджЪМјБ№ЃК ЗжБ№ШЁЕШЬхЛ§ЦјЬхГЦжЪСПЃЌжЪСПДѓЕФЪЧЖўбѕЛЏЬМЃЌжЪСПаЁЕФЪЧбѕЦј
РћгУЛЏбЇаджЪМјБ№ЃК
НЋШМзХЕФФОЬѕЩьШыбљЦЗжаЃЌШМЩеИќЭњЕФЪЧбѕЦјЃЌЯЈУ№ЕФЪЧЖўбѕЛЏЬМ
2дкЖдРЏжђМАЦфШМЩеНјааСЫЬНОПвдКѓЃЌЧыФуЬюаДЯТСаПеИёЃК
ЃЈ1ЃЉФФаЉЪЧашвЊШМЩеВХФмЙлВьЕНЕФЯжЯѓЃЈЬюађКХЃЉ ЂлЂоЂпЂсЂт
ЂйздЖЅЖЫЦ№дМ1cmвдФкЕФжђЬхЪЧЮТЕФЁЂШсШэЧввзЫмаЭЃЛ
ЂкдСЯЪЧАыЭИУїЁЂЮЂГєЁЂЮоЮЖАзЩЋЙЬЬхЃЛ
ЂлРЏжђЖЅЖЫЁЂжђаФЕзВПжмЮЇгаЮоЩЋвКЬхЃЌГЪЭызДДцдкЃЛ
ЂмвЛАзЩЋжђаФЙсДЉжажсЃЌВЂбгГЄжСРЏжђЖЅ1cmЃЛ
ЂнаЮзДдВжљаЮЃЌЖЅВПЮЊдВзЖаЮМтГіЃЛ
ЂожђаФжмЮЇКЭжђбцЩЯЖЫГЪУїССЕФЛЦЩЋЃЛ
ЂпДЕЯЈКѓЃЌФмПДМћжђаФжмЮЇгаАзбЬЩЯЩ§ЃЌВЂТ§Т§ЯћЪЇЃЛ
ЂржЪШэЃЌПЩгУжИМзЙЮГіКлМЃЃЛ
ЂсШєЗчДЕжСРЏжђвЛБпЃЛСэвЛБпЭыаЮЖЅЖЫЕФРЏжђНЋШлГЩвКЬхВЂбижђЬхТфЯТЃЛ ЂтШчЪмПеЦјСїЕФгАЯьЃЌЛ№бцЛсЩСЖЏЃЌЧвЩњГіКкбЬЃЎ
ЃЈ2ЃЉШЁвЛжЇРЏжђЃЌгУаЁЕЖЧаЯТвЛаЁПщЃЌАбЫќЗХШыЫЎжаЃЌРЏжђЛсИЁдкЫЎУцЩЯ НсТлЃКЪЏРЏЕФУмЖШБШЫЎаЁ
ЃЈ3ЃЉдйНЋвЛжЛИЩдяЕФЩеБеждкРЏжђЛ№бцЩЯЗНЃЌЩеБФкБкГіЯжЫЎЮэЃЌЦЌПЬКѓШЁЯТЩеБЃЌбИЫйЯђЩеБФкЕЙШыЩйСПГЮЧхЕФЪЏЛвЫЎЃЌеёЕДКѓЗЂЯжГЮЧхЪЏЛвЫЎБфЛызЧ
НсТлЃКРЏжђШМЩевдКѓЕФЩњГЩЮяЪЧЫЎКЭЖўбѕЛЏЬМ
дкЖдРЏжђМАЦфШМЩеНјааСЫЬНОПвдКѓЃЌЧыФуЬюаДЯТСаПеИёЃК
ЃЈ1ЃЉШЁвЛжІРЏжђЃЌгУаЁЕЖЧаЯТвЛаЁПщЃЌАбЫќЗХШыЫЎжаЃЌРЏжђЛс ИЁдкЫЎУц НсТлЃКЪЏРЏЕФУмЖШБШЫЎаЁ
ЃЈ2ЃЉЕуШМРЏжђЃЌЙлВьЕНРЏжђЛ№бцЗжЮЊШ§ВуЃЌЗжБ№ЪЧЭтбцЁЂФкбцЁЂбцаФЃЌАбвЛИљЛ№ВёЙЃЗХдкРЏжђЕФЛ№бцЩЯдМ1SКѓШЁГіЃЌПЩвдПДЕНaДІЃЈЬюзжФИЃЉЕФЛ№ВёЙЃзюЯШЬМЛЏЃЎ
НсТлЃКРЏжђЛ№бцЕФ ЭтбцЮТЖШзюИпЃЎ
ЃЈ3ЃЉдйНЋвЛжЛИЩдяЕФЩеБеждкРЏжђЛ№бцЕФЩЯЗНЃЌЩеБФкБкГіЯжЫЎЮэ
ЦЌПЬКѓШЁЯТЩеБЃЌбИЫйЯђЩеБФкЕЙШыЩйСПЕФГЮЧхЪЏЛвЫЎЃЌеёЕДКѓЗЂЯжГЮЧхЪЏЛвЫЎБфЛызЧ
НсТлЃЛРЏжђШМЩевдКѓЕФЩњГЩЮяЪЧЖўбѕЛЏЬМКЭЫЎ
4ПЩгУгкЬюГфЬНПеЦјЧђКЭзїКИНгН№ЪєБЃЛЄЦјЕФЮяжЪЪЧ КЄЦјЃЎ
аЁАќзАИтЕуРрЪГЦЗГЃВЩгУГфЦјАќзАЃЌЕЊЦјЪЧГЃгУЕФГфЬюЦјЬхЃЎЧыФуИљОнЕЊЦјЕФаджЪаДГібЁгУЕЊЦјЕФжївЊдвђЪЧЕЊЦјЕФЛЏбЇаджЪВЛЛюЦУЃЌЮоЖО
ЃЈ1ЃЉЯЁгаЦјЬхПЩгУгкБЃЛЄЦјЪЧРћгУСЫЦф ЛЏбЇаджЪМЋВЛЛюЦУЕФаджЪЃЌ
ЃЈ2ЃЉбѕЦјПЩгУгкгюКНКЭЧБЫЎЪЧРћгУСЫЦфФмЙЉИјКєЮќЕФаджЪЃЌ
ЃЈ3ЃЉЯЁгаЦјЬхгУгкЕчЙтдДЪЧРћгУСЫЦфЮяРэЃЈЬюЁАЮяРэЁБЛђЁАЛЏбЇЁБЃЉаджЪЃЌ
ЃЈ4ЃЉРћгУЗжРывКЬЌПеЦјЗЈжЦбѕЦјЪЧРћгУСЫПеЦјжаЕЊЦјКЭбѕЦјЗаЕуВЛЭЌЕФаджЪЃЎ 5ЫЎгаЯТЪіаджЪЃКЂйЫЎЪЧУЛгабеЩЋЁЂУЛгаЦјЮЖЁЂУЛгаЮЖЕРЕФЭИУївКЬхЃЛЂкЫЎЭЈЕчЛсгаЧтЦјЁЂбѕЦјЗХГіЃЛЂлМгШШжС100ЁуCЫЎЛсБфГЩЫЎеєЦјЃЛЂмвЛаЉбѕЛЏЮяФмШмгкЫЎЩњГЩЫсЛђМюЕШЮяжЪЃЎЦфжаЪєгкЫЎЕФЛЏбЇаджЪЕФЪЧ ЂкЂмЃЈгУБрКХЬюаДЃЉЃЎ
6.2004Фъ5дТ25ШеЮвЪаФГЕиЗЂЩњСЫвЛЦ№бЧЯѕЫсФЦжаЖОЪТМўЃЎбЧЯѕЫсФЦЭтЙлПсЫЦЪГбЮЧвгаЯЬЮЖЃЌбЧЯѕЫсФЦКЭЪГбЮЕФгаЙизЪСЯШчЯТЃК
Яю ФП бЧЯѕЫсФЦЃЈNaNO2ЃЉ ТШЛЏФЦЃЈNaClЃЉЫЎШмад взШмЃЌдк15ЁцЪБШмНтЖШЮЊ81.5g взШмЃЌдк15ЁцЪБШмНтЖШЮЊ35.8gШл Еу 271Ёц 801ЁцЗа Еу 320ЁцЛсЗжНтЃЌЗХГігаГєЮЖЕФЦјЬх 1413ЁцИњЯЁбЮЫсзїгУ ЗХГіКьзиЩЋЕФЦјЬхNO2 ЮоЗДгІ
ЃЈ1ЃЉИљОнЩЯБэЧыФуаДГібЧЯѕЫсФЦЕФСНЬѕЮяРэаджЪ взШмгкЫЎЃЌ ШлЕу271ЁцЃЎ
ЃЈ2ЃЉаДГіМьбщЪГбЮжаЪЧЗёКЌгабЧЯѕЫсФЦЕФЙ§ГЬ
ЗНЗЈвЛЃКШЁЩйСПД§ВтЪГбЮгыЯЁбЮЫсЗДгІЃЌШєгаКьзиЩЋЦјЬхВњЩњЃЌдђИУЪГбЮжаЛьгабЧЯѕЫсФЦЃЛЗДжЎдђЮоЃЎ
ЗНЗЈЖўЃКШЁД§ВтЪГбЮМгШШЕН320ЁцвдЩЯЃЌШєгаГєЮЖЦјЬхВњЩњЃЌдђЪГбЮжаКЌгабЧЯѕЫсФЦЃЛЗДжЎдђЮоЃЎ
7.ЮоЩЋЛьКЯЦјЬхПЩФмКЌгаЫЎеєЦјЁЂвЛбѕЛЏЬМЁЂЖўбѕЛЏЬМЁЂТШЛЏЧтЁЂЧтЦјЃЎЕБЛьКЯЦјЬхЭЈЙ§ХЈСђЫсКѓЦјЬхЬхЛ§УЛгаБфЛЏЃЛдйЭЈЙ§зуСПГЮЧхЪЏЛвЫЎКѓЃЌвВУЛгаГіЯжУїЯдБфЛЏЃЌЕЋЦјЬхЬхЛ§МѕЩйвЛАыЃЛЕуШМЕМГіЕФЮВЦјЃЌНЋШМЩеВњЮяЭЈЙ§ЮоЫЎСђЫсЭВЛБфЩЋЃЌШДФмЪЙГЮЧхЪЏЛвЫЎБфЛызЧЃЎдђЛьКЯЦјЬхжаПЯЖЈгавЛбѕЛЏЬМЁЂТШЛЏЧтЃЌПЯЖЈУЛгаЫЎеєЦјЁЂЖўбѕЛЏЬМЁЂЧтЦјЃЎ
8ЮЊСЫжЄУїФГЮяжЪШМЩеКѓЪЧЗёЩњГЩЫЎКЭЖўбѕЛЏЬМЃЌзіСЫШчЯТЪЕбщЃЌЧыВЙГфЭъећЃЎ
дкЯТСаЮяжЪжабЁдёЪЪЕБЮяжЪЬюПеЃЈЬюзжФИЃЉЃК
AЁЂПеЦјBЁЂЖўбѕЛЏСђCЁЂКьСзDЁЂЮхбѕЛЏЖўСзEЁЂЫЎFЁЂбѕЦјGЁЂЕЊЦјЃЎ
ЃЈ1ЃЉФмЪЙДјЛ№аЧФОЬѕИДШМЕФЦјЬх F
ЃЈ2ЃЉЮоЩЋгаДЬМЄадЦјЮЖЕФЦјЬхЪЧ B
ЃЈ3ЃЉдкбѕЦјжаЗДгІЃЌВњЩњДѓСПАзбЬЕФЪЧC
ЃЈ4ЃЉЪєгкЛьКЯЮяЕФЪЧA
ЃЈ5ЃЉЪєгквзШМЮяЕФЪЧ
ЃЈ2011?зЭВЉЃЉОпБИЛљБОЕФЛЏбЇЪЕбщММФмЪЧНјааЛЏбЇЬНОПЛюЖЏЕФЛљДЁКЭБЃжЄЃЌЭЌЪБвВЗДгГСЫЪЕбщепЕФЛЏбЇбЇПЦЫибјЃЌвдЯТЪЕбщВйзїе§ШЗЕФЪЧЃЈ ЃЉ
ЃЈ2011?жиЧьЃЉЯТЭМЫљЪОЕФЛЏбЇЪЕбщЛљБОВйзїе§ШЗЕФЪЧЃЈ ЃЉ
ЃЈ2011?еиЧьЃЉЯТСаЪЕбщВйзїВЛе§ШЗ ЕФЪЧЃЈ ЃЉ
ЃЈ2011?еПНЃЉЯТЭМЫљЪОЕФЪЕбщВйзїЕФЭМЪОжаЃЌе§ШЗЕФЪЧЃЈ ЃЉ
ЃЈ2011?ЮоЮ§ЃЉЯТСаЪЕбщВйзїе§ШЗЕФЪЧ ЃЈ ЃЉ
ЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈ,вВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈЦЊЖўЃКАЫЯТПЦбЇЭиеЙСЗЯАЫФ
АЫЯТПЦбЇЭиеЙСЗЯАЫФ
ЁЊЁЊПеЦјКЭбѕЦј
вЛЃЎЦјЬхЕФЪЕбщЪвжЦЗЈ
1ЃЎ бЁдёЦјЬхЪЕбщЪвжЦЗЈЕФдРэЪБашвЊПМТЧЃК ЁЃ
2ЃЎбЁдёЦјЬхЗЂЩњзАжУЕФвРОнЪЧ ЁЃ
3ЃЎбЁдёЦјЬхЕФЪеМЏзАжУЕФвРОнЪЧ ЁЃ ЯАЬт
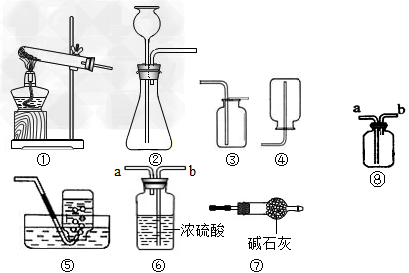
1ЃЎЯТСазАжУВйзїЭМВЛФмгУгкМьВщЦјУмадЕФЪЧ
2ЃЎЯТЭМЪЧЪЕбщЪвжЦШЁЦјЬхЕФвЛаЉзАжУЃЌОнЭМЛиД№гаЙиЮЪЬтЁЃ(гбЧщЬсЪОЃКвдЯТЫљбЁзАжУОљЬюзАжУађКХ
(1)аДГіжИЖЈвЧЦїЕФУћГЦЃК
ЂйЃЛЂкЃЛ
(2)аДГівЛИіГѕжаЛЏбЇжагУзАжУCжЦЦјЬхЕФЛЏбЇБэДяЪНЪеМЏДЫЦјЬхПЩбЁгУЕФвЛжжзАжУЪЧ ЃЌРћгУИУзАжУЛЙФмЪеМЏЕФвЛжжЦјЬхЪЧЃЛ
(3) ЪЕбщЪвдкГЃЮТЯТгУПщзДЕчЪЏгыЫЎЗДгІжЦШЁЮЂШмгкЫЎЕФввШВЦјЬхЃЌИУЗДгІБиаыбЯИёПижЦМгЫЎЫйЖШЃЌвдУтОчСвЗДгІЗХШШв§Ц№ЗЂЩњзАжУеЈСбЁЃФуШЯЮЊЩЯЭМжазюЪЪКЯжЦШЁввШВЦјЬхЕФЗЂЩњзАжУЪЧ ЃЛШчЙћгУгвЭМЫљЪОзАжУЪеМЏввШВЃЌЦјЬхгІДг
(ЬюЁАaЁБЛђЁАbЁБ)ЖЫЙмПкЭЈШЫЁЃ
ЃЈ4ЃЉМзЭщЪЧвЛжжЮоЩЋЁЂЮоЮЖЃЌФбШмгкЫЎЃЌУмЖШБШПеЦјаЁЕФЦјЬхЁЃаЁСсгУМгШШДзЫсФЦКЭМюЪЏЛв(ОљЮЊЙЬЬх)ЕФЗНЗЈжЦШЁМзЭщЃЌаЁСсгІбЁдёжЦШЁМзЭщЕФЗЂЩњКЭЪеМЏзАжУЪЧ (ЬюађКХ)ЁЃШєгУгвЭМзАжУЪеМЏМзЭщЃЌМзЭщгІДг ЖЫНјШы(бЁЬюЁАAЁБЛђЁАBЁБ)ЁЃ
ЃЈ5ЃЉСђЛЏЧтЃЈH2SЃЉЪЧвЛжжгаЖОЦјЬхЃЌЦфУмЖШБШПеЦјДѓЃЌЧвФмШмгкЫЎЃЌЫЎШмвКГЪЫсадЁЃЃЎЃЎ
ЪЕбщЪвЭЈГЃгУСђЛЏбЧЬњЃЈFeSЃЉгыЯЁСђЫсдкГЃЮТЯТЭЈЙ§ИДЗжНтЗДгІжЦЕУЁЃаЁЛЊЭЌбЇЩшМЦЕФЪЕбщзАжУЮЊBDзщКЯЃЌФуШЯЮЊДЫзАжУЪЧЗёКЯРэЃЈЬюЁАКЯРэЁБЛђЁАВЛКЯРэЁБЃЉЃЌРэгЩЪЧЁЃШчКЮЪеМЏСђЛЏЧтЃЈH2SЃЉЃП
ЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈЃЌвВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈЁЃ
ЃЈ6ЃЉЙщФЩГіЪЕбщЪвжЦШЁЦјЬхЗДгІЕФЙВЭЌЕу ЃЈЬюађКХЃЉЁЃ
ЂйашвЊМгШШ ЂкЪЙгУДпЛЏМС ЂлУЛгаЦјЬхВЮМгЗДгІ ЂмдСЯЮЊДПОЛЮя ЂнжЛЩњГЩвЛжжЦјЬх
ЖўЃЎ ПеЦјЁЂO2ЕФЯрЙижЊЪЖМАЭиеЙ
ЃЈвЛЃЉПеЦјГЩЗжЕФВтЖЈЃК ЭиеЙЃКХчШЊЪЕбщЪЧвЛИіИЛгаЬНЫївтвхЕФЪЕбщЃЌдкИпжа
ЛЏбЇНЬбЇжаОпгаживЊЕФЕиЮЛЁЃЪЕбщЕФЛљБОдРэЪЧЪЙЩеЦПФкЭтдкЖЬЪБМфФкВњЩњНЯ
ДѓЕФбЙЧПВюЃЌРћгУДѓЦјбЙНЋЩеЦПЯТУцЩеБжаЕФвКЬхбЙШыЩеЦПФкЃЌдкМтзьЕМЙмПк
аЮГЩХчШЊЃЈШчЭМ2ЃЉЁЃетРрЪЕбщЕФвЊЧѓЪЧЃКЂйзАжУЦјУмадСМКУЃЛЂкЫљгУЦјЬхФмЃЎЃЎЃЎ
ДѓСПШмгкЫљгУвКЬхЛђЦјЬхгывКЬхПьЫйЗДгІЁЃЃЈИКбЙдРэЃЉ ЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎЃЎ
ПеЦјГЩЗжЕФВтЖЈжївЊЪЧРћгУИУдРэЃЌЧыЩшМЦГіВЛЭЌЕФЗНАИВтЖЈПеЦјЕФГЩЗж
ИКбЙдРэЕФЮЃКІ
Р§ШчЃКЪЕбщЪвгУИпУЬЫсМижЦШЁбѕЦјЪЕбщНсЪјКѓЃЌШчЯШвЦзпОЦОЋЕЦЃЌКѓвЛвЦзпЕМЙмЛсгаЕЙЮќЯжЯѓЕФЗЂЩњ
1ЃЎЮЊЪВУДЪЕбщНсЪјКѓЃЌЛсгаЕЙЮќЯжЯѓЕФЗЂЩњЃП
2ЃЎШчКЮЗРжЙЕЙЮќЯжЯѓЕФЗЂЩњЃП
1ЃЎгУРДВтЖЈПеЦјГЩЗжЕФЗНЗЈКмЖрЃЌЭМ1ЫљЪОЕФЪЧгУКьСздкПеЦјжаШМЩеЕФ
ВтЖЈЗНЗЈЁЃЪЕбщЙ§ГЬЪЧЃК
ЕквЛВНЃКНЋМЏЦјЦПШнЛ§ЛЎЗжЮЊЮхЕШЗнЃЌВЂзіКУБъМЧЁЃ
ЕкЖўВНЃКЕуШМШМЩеГзФкЕФКьСзЃЌЩьШыМЏЦјЦПжаВЂАбШћзгШћНєЁЃ
ЕкШ§ВНЃКД§КьСзЯЈУ№ВЂРфШДКѓЃЌДђПЊЕЏЛЩМаЃЌЗЂЯжЫЎБЛЮќ
ШыМЏЦјЦПжаЃЌНјШыМЏЦјЦПжаЫЎЕФЬхЛ§дМЮЊМЏЦјЦПзмШнЛ§ЕФ1/5ЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЩЯУцЕФЪЕбщЭЌЪБжЄУїСЫЕЊЦјгаЕФЛЏбЇаджЪЁЃ
ЭМ1 ЃЈ2ЃЉМзЭЌбЇЕФЙуПкЦПФкЫЎУцЩЯЩ§УїЯдаЁгкЦПФкПеЦјЬхЛ§ЕФ1/5ЃЌввЭЌбЇЕФ
ЙуПкЦПФкЫЎУцЩЯЩ§УїЯдДѓгкЦПФкПеЦјЬхЛ§ЕФ1/5ЁЃЯТСаЖдетСНжжЯжЯѓНтЪЭКЯ
РэЕФЪЧ
ЂйМзЭЌбЇПЩФмЪЙгУКьСзЕФСПВЛзуЃЌЦПФкбѕЦјУЛгаЯћКФЭъ
ЂкМзЭЌбЇПЩФмЮДШћНєЦПШћЃЌКьСзЯЈУ№РфШДЪБЭтНчПеЦјНјШыЦПФк
ЂлввЭЌбЇПЩФмУЛМаНєЕЏЛЩМаЃЌКьСзШМЩеЪБЦПФкВПЗжПеЦјЪмШШДгЕМЙмвнГі
ЂмввЭЌбЇПЩФмВхШыШМЩеГзЬЋТ§ЃЌШћНєЦПШћжЎЧАЃЌЦП
ФкВПЗжПеЦјЪмШШвнГі
AЁЂжЛгаЂйЂл BЁЂжЛгаЂкЂмCЁЂжЛгаЂйЂкЂлDЁЂжЛгаЂйЂкЂлЂм
ЃЈ3ЃЉФГЭЌбЇЖдЪЕбщНјааЗДЫМКѓЃЌЬсГіСЫИФНјЗНЗЈЃЈШчЭМ2ЫљЪО ЃЉЃЌФуШЯЮЊИФНјКѓЕФгХЕуЪЧЃК
2
ЃЎаЁДЯКЭаЁУїЖджёзгжаЦјЬхЕФГЩЗжНјааЬНОПЁЃЫћУЧАбжё
згНўХндкЫЎжаЃЌдкжёзгЩЯзъСЫвЛИіаЁПзЃЌПДЕНгаЦјХнДгаЁПзжаУАГіЃЌОЭгУ
_______________ЗЈЪеМЏСЫСНЦПЦјЬхЁЃ
ЕквЛЦПЃКВЩгУгвЭМЫљЪОЕФЗНЗЈЕуШМКьСзЃЌгаАзбЬЩњГЩЁЃАбзАжУЗХдкЫЎжаЃЌДђ
ПЊжЙЫЎМаЃЌНјШыМЏЦјЦПЕФЫЎдМеММЏЦјЦПЬхЛ§ЕФ1/10ЁЃ
ЕкЖўЦПЃКЕЙШыЩйСПГЮЧхЕФЪЏЛвЫЎЃЌеёЕДЃЌЪЏЛвЫЎБфЛызЧЁЃ
гЩДЫЭЦЖЯЃКжёзгжаКЌга_______________ЦјЬх ЁЃ
ЭЈЙ§ЪЕбщЃЌЫћУЧНЋжёзгжаСНжжЦјЬхЕФКЌСПгыПеЦјНјааСЫБШНЯЃЌЕУГіЕФНсТлЪЧ_____________ЁЃ
ЃЈЖўЃЉбѕЦјЕФжЦШЁ
1ЃЎЮЊСЫжЦБИЩйСПЕФбѕЦјЃЌФГЪЕбщаЁзщЗжШ§ИіНзЖЮПЊеЙСЫвЛЯЕСаЕФЙЄзїЃК
ЕквЛНзЖЮЃКВщдФЮФЯззЪСЯЃЌЛёЕУСЫЯТСааХЯЂЃКЫЋбѕЫЎЁЂТШЫсМиЁЂИпУЬЫсМиЕШКЌгабѕдЊЫиЕФЮяжЪдквЛЖЈЕФЬѕМўЯТЗжНтЖМПЩвдВњЩњбѕЦјЁЃЦфжаЫЋбѕЫЎШмвКМлИёзюЕЭЃЌдкГЃЮТЯТОЭФмЙЛЗжНтЗХГібѕЦјЃЌИУЙ§
ГЬЮоИБВњЮяЃЛТШЫсМиМлИёНЯИпЃЌЗжНтНЯРЇФбЃЌЧвГЃАщгаИБВњЮяЃЛИпУЬЫсМиМлИёНЯИпЃЌМгШШМДПЩПьЫйЗжНтЁЃЖўбѕЛЏУЬФмМгЫйЩЯЪіШ§жжЮяжЪЕФЗжНтЁЃ
ИљОнЩЯЪіаХЯЂЃЌбЁдёЫЋбѕЫЎШмвККЭЖўбѕЛЏУЬЛьКЯжЦБИбѕЦјЁЃ
ЕкЖўНзЖЮЃКЕНЪЕбщЪвзМБИЪЕбщгУЦЗЃЌАВзАЪЕбщвЧЦїЃЌНјаажЦБИЪЕбщЁЃПЩЙЉбЁдёЕФЪЕбщзАжУШчЯТЃК
ЕкШ§НзЖЮЃКЪЕбщЭъБЯОЃЌЯДЫЂЪЕбщвЧЦїЃЌећРэЪЕбщгУЦЗЁЃ
ЮЪЬтЃК
(1)вЊжЦШЁвЛЦПбѕЦјЃЌгІбЁдёЕФЪЕбщзАжУЪЧ_________________(ЬюаДзжФИДњКХ)ЃКзщзАКУЪЕбщзАжУКѓгІЪзЯШНјаа____________________________________ЁЃ
(2)гаЦјЬхВњЩњЕФЛЏбЇЗДгІдкгаЯоЕФПеМфРяЗЂЩњЪБЃЌШчЙћЗДгІЙ§ПьЃЌШнвзв§Ц№БЌеЈЃЌФуШЯ ЮЊПЩвдВЩШЁФФаЉДыЪЉдЄЗРБЌеЈЃП(СаОйСНЬѕ)____________________________________ЁЃ
(3)ЛиЙЫећИіЙЄзїЙ§ГЬЃЌФуШЯЮЊдкзМБИЙЄзїНзЖЮГ§гІПМТЧвЉЦЗЕФМлИёЁЂжЦбѕЗДгІЕФФбвзЁЂжЦбѕЙ§ГЬЕФАВЗжадЕШЮЪЬтЭтЃЌЛЙгІПМТЧФФаЉЮЪЬтЃП(жСЩйСаОйСНЬѕ)
______________________________________________________________________ЁЃ
2ЃЎЙ§ШЅНЬВФжаЪЕбщЪвжЦбѕЦјЃЌГЃгУТШЫсМигыЖўбѕЛЏУЬЛьКЯМгШШжЦШЁЃЌзАжУШчЭМЫљЪОЃЌДгдЄШШЕНЪеМЏТњвЛЦП(250mL)бѕЦјДѓдМаш8ЁЋ10ЗжжгЃЌДгЗДгІКѓЪЃгрЕФЙЬЬхжаЛиЪеЖўбѕЛЏУЬБШНЯРЇФбЃЌдјгаЭЌбЇШЅЮХздМКЪеМЏЕНЕФбѕЦјЃЌЯыевевЮќбѕЕФИаОѕЃЌНсЙћШДЮХЕНДЬМЄадЦјЮЖ(ЩйСПТШЫсМиЗЂЩњИБЗДгІЩњГЩгаЖОЕФТШЦј)ЁЃ
ЯжааНЬВФвбИФгУЙ§бѕЛЏЧтШмвККЭЖўбѕЛЏУЬЛьКЯжЦШЁбѕЦјЃЌФуШЯЮЊетбљзіЕФгХЕуЖМгаФФаЉ?(1) ЃЛ(2) ЃЛ(3)ЃЛ(4) ЁЃ
ЃЈШ§ЃЉДпЛЏМС
1ЃЎПЮЬУЩЯЭЌбЇУЧРћгУМзЭМзАжУзіЙ§бѕЛЏЧтЗжНтЪЕбщЪБЃЌ
ДјЛ№аЧЕФФОЬѕКмФбИДШМЃЌгкЪЧРЯЪІМгСЫвЛИіUаЮЙмЃЌШчвв
ЭМЃЌДјЛ№аЧЕФФОЬѕНЯвзИДШМЁЃ
ЧыЛиД№ЃК
(1)аДГіЪЕбщЪвжЦШЁбѕЦјЕФЛЏбЇЗДгІБэДяЪНЃКЁЃ
(2)ИФгУввзАжУКѓФмЪЙДјЛ№аЧЕФФОЬѕИДШМЕФдвђЃК
(3)ИљОн(2)жаЭЦВтЕФдвђЃЌЧыФуЩшМЦвЛИіаТЕФИФНјзАжУ(ПЩгУЭМЪОЛђгУЮФзжа№ЪіИФНјвЊЕу)ЁЃ
2ЃЎПЦбЇЪЕбщжЄУїЃКПеЦјжаЮЂСПГєбѕЃЈO3ЃЉПЩЕжПЙбєЙтжазЯЭтЯпЖдШЫЬхЫ№КІЃЌзїПеЕїКЭБљЯфЕФжТРфМСЁАЗњРяАКЁБЪЧвЛжжТШЗњЬўЃЈвдmДњЬцЦфЛЏбЇЪНЃЉЃЌЫќПЩЦЦЛЕГєбѕВуЃЌЦфЗДгІЙ§ГЬПЩБэЪОЮЊЃКm+O3Ёњm
ЃЌmmЃЌИљОнЫљбЇжЊЪЖПЩжЊТШЗњЬўдкЗДгІжаЕФзїгУЪЧЃЈ ЃЉ
ЃЈAЃЉбѕЛЏМС ЃЈЃТЃЉЛЙдМСЃЈCЃЉДпЛЏМСЃЈDЃЉЮШЖЈМС
3ЃЎЦЎГОЪЧЮяжЪШМЩеЪБВњЩњЕФСЃзДЦЎИЁЮяЃЌПХСЃКмаЁЃЌВЛвзГСНЕЁЃЫќгыПеЦјжаЕФSO2ЁЂO2НгДЅЪБЃЌSO2ЛсВПЗжзЊЛЏЮЊSO3ЃЌЪЙПеЦјЕФЫсЖШдіМгЁЃЦЎГОЫљЦ№ЕФзїгУПЩФмЪЧ ( )
(A)бѕЛЏМС (B)ЛЙдМС (C)ДпЛЏМС (D)ЮќИНМС
4ЃЎбЇаЃЛЏбЇаЫШЄаЁзщжЊЕРЖўбѕЛЏУЬФмзїЙ§бѕЛЏЧтЗжНтЕФДпЛЏМСКѓЃЌдйЯыЬНОПЦфЫћвЛаЉЮяжЪШчбѕЛЏТСЪЧЗёвВПЩзїЙ§бѕЛЏЧтЗжНтЕФДпЛЏМСЁЃЧыФувЛЦ№ВЮгыЫћУЧЕФЬНОПЙ§ГЬЃЌВЂЬюаДЯТСаПеАзЁЃ
(1)[ЮЪЬт]Al2O3ФмВЛФмзїЙ§бѕЛЏЧтЗжНтЕФДпЛЏМСФи?
(2)[ВТЯы]Al2O3ФмзїЙ§бѕЛЏЧтЗжНтЕФДпЛЏМСЁЃ
2323(5)[ЬжТлгыЗДЫМ]ОЙ§ЬжТлЃЌгаЕФЭЌбЇШЯЮЊжЛгаЩЯЪіСНИіжЄОнЃЌВЛФмжЄУїAl2O3ФмзїЙ§бѕЛЏЧтЗжНтЕФДпЛЏМСЃЌЛЙвЊВЙГфвЛИіЬНОПЪЕбщЃК
ЪЕбщШ§ЃК[ЪЕбщФПЕФ]ЬНОП
[ЪЕбщВНжш]ЂйзМШЗГЦСПAl2O3(ЩйСП)ЕФжЪСПЃЛЂкЭъГЩЪЕбщЖўЃЛЂлД§ЗДгІНсЪјЃЌНЋЪЕбщЖўЪдЙмРяЕФЮяжЪНјааЙ§ТЫЃЌЯДЕгЃЌ ЃЌГЦСПЃЛЂмЖдБШЗДгІЧАКѓAl2O3ЕФжЪСПЁЃ
[ЬжТл]ШчЙћAl2O3дкЗДгІЧАКѓжЪСПВЛБфЃЌдђЫЕУїAl2O3ПЩвдзїЙ§бѕЛЏЧтЗжНтЕФДпЛЏМСЁЃ
(6)ЕЋаЁЛЊШЯЮЊЃЌвЊжЄУїВТЯыЃЌЩЯЪіШ§ИіЪЕбщЛЙВЛзуЙЛЃЌЛЙашвЊдйдіМгвЛИіЬНОПЪЕбщЃКЬНОПЁЃ
ЃЈЫФЃЉЁЂЦфЫћ
1ЃЎДђРзЗХЕчЪБЃЌПеЦјжагаМЋЩйСПбѕЦјЛсзЊЛЏГЩГєбѕЃЈ3O2 = 2O3ЃЉЃЌЯТСагаЙиЫЕЗЈжае§ШЗЕФЪЧ ( )
(A)ИУБфЛЏЪЧЮяРэБфЛЏ (B)O2гыO3ЖМЪЧЕЅжЪ
(C)O2гыO3ЪЧВЛЭЌЕФЮяжЪ (D)O2гыO3ЕФаджЪЭъШЋЯрЭЌ
2.ОнБЈЕРЃКФГЕивЛУћ5ЫъЕФХЎКЂзгАбЭПИФвКЕБвћСЯЮќЪГЃЌЪГЕРБЛбЯжиЩеЩЫЁЃОвНдКМьВтКѓЗЂЯжЃЌЭПИФвКжаКЌгаБНЁЂМзЛљЛЗвбЭщЕШЖржжгаЖОЮяжЪЁЃгЩДЫПЩжЊЃЌЭПИФвКЪЧЃЈ ЃЉ
AЁЂЛьКЯЮя BЁЂДПОЛЮяCЁЂЕЅжЪ DЁЂЛЏКЯЮя
3. ЯТСаЮяжЪгыбѕЦјЗДгІЫљЕУЕФВњЮядкГЃЮТЯТЮЊЦјЬхЕФЪЧЃЈ ЃЉ
AЃЎЬМ BЃЎСз CЃЎЬњ DЃЎУО
4. НёФъЁАСљЁЄЮхЁБЪРНчЛЗОГШежаЙњжїЬтЪЧЁАЮлШОМѕХХгыЛЗОГгбКУаЭЩчЛсЁБЁЃЭЦЖЏЮлШОМѕХХЁЂНЈЩшЛЗОГгбКУаЭЩчЛсЪЧШЋЩчЛсЙВЭЌЕФд№ШЮЁЃЯТСаЮяжЪжаЃЌЪєгкДѓЦјжївЊЮлШОЮяЃЌБиаыМѕЩйХХЗХЕФЪЧЃЈ ЃЉ
AЃЎSO2 BЃЎCO2 CЃЎN2 DЃЎO2
5. ЫЎЪЧЩњУќЕФдДШЊЃЌЯТСаЁАЫЎЁБжаЪєгкДПОЛЮяЕФЪЧЃЈ ЃЉ
AЁЂгъЫЎ BЁЂздРДЫЎ CЁЂеєСѓЫЎDЁЂПѓШЊЫЎ
12. ЁАЩёжл6КХЁБЬЋПеВеРћгУNiFe2O4НЋКНЬьдБКєГіЕФCO2зЊЛЏЮЊO2ЃЌЖјNiFe2O4ЕФжЪСПКЭЛЏбЇаджЪЖМВЛБфЁЃдђNiFe2O4дкИУЙ§ГЬжаЪЧЃЈ ЃЉ
AЃЎЗДгІЮя BЃЎЩњГЩЮя CЃЎДпЛЏМС DЃЎЯћЖОМС
13ЃЎФГзЈгУЪЕбщЪввЊПижЦЪвФкПеЦјжабѕЦјЕФКЌСПЁЃЯжашвЊЖдЪвФкЕФПеЦјШЁбљМьбщЃЌЧыФуЩшМЦГізюМђБуЕФЗНЗЈЃЌШЁГіЪвФкЕФПеЦјбљЦЗЁЃЙЉбЁгУЕФЪЕбщгУЦЗгаЃКЩеБЁЂМЏЦјЦПЁЂЫЎВлЁЂТЉЖЗЁЂСПЭВЁЂЯ№ЦЄЙмЁЂВЃСЇЦЌЁЂЫЎЁЃ
ЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈ,вВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈЦЊШ§ЃК16.04ЦкжаЛЏбЇ
2015ЁЊ2016бЇФъЖШЕкЖўбЇЦкЕкЖўДЮФЃФтЪдЬт
ФъМЖОХФъМЖ ПЦФПЛЏбЇ
CЃЎЫцвтЖЊЦњЗЯОЩЕчГи DЃЎПЊЗЂРћгУЧхНрФмдД
8ЃЎгюжцЗЩДЌФкЃЌгУКЌЧтбѕЛЏяЎЕФЙ§ТЫЭјГ§ШЅгюКНдБКєГіЕФЖўбѕЛЏЬМЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК2LiOH+CO2 ==Li2CO3+XЃЌдђXЕФЛЏбЇЪНЮЊЃЈ ЃЉ
2
2
2
2
AЃЎH BЃЎO CЃЎHO DЃЎN
ПЩФмгУЕНЕФЯрЖддзгжЪСПЃК C-12 H-1O-16Na-23 Cl-35.5Ca-40
вЛЁЂбЁдёЬт(УПаЁЬтжЛга1ИібЁЯюЗћКЯЬтвтЁЃЙВ10ИіаЁЬтЃЌУПаЁЬт2ЗжЃЌЙВ20ЗжЁЃ) 9ЃЎжЛгУвЛжжЯТСаЪдМСВЛФмМјБ№ЯЁСђЫсЁЂТШЛЏФЦКЭЧтбѕЛЏБЕШ§жжЮоЩЋШмвКЕФЪЧ ЃЈ ЃЉ AЃЎpHЪджН BЃЎЯЁбЮЫс CЃЎзЯЩЋЪЏШяЪдвК DЃЎЬМЫсФЦШмвК
1ЃЎЩњЛюжагаЬЋЖрЕФБфЛЏ,ЯТСаЁББфЛЏЁБжаЩцМАЛЏбЇБфЛЏЕФЪЧЃЈ ЃЉ
AЃЎЪїИљЁАБфЁБИљЕёBЃЎЦЯЬбЁАБфЁБУРОЦ CЃЎгёЪЏЁАБфЁАгЁеТDЃЎЭцОпЛњЦїШЫЁАБфЁБаЮ
2ЃЎЁАгХЛЏЛЗОГЁЂЗРжЙЮлШОЁБвбГЩЮЊЮвУЧЕФЙВЪЖЁЃЯТСазіЗЈжаЃЌФуШЯЮЊДэЮѓЕФЪЧЃЈЃЉ A.ЙЄГЇжБНгХХЗХЕФSO2ЁЂNO2ЕШЦјЬхЛсЮлШОПеЦј B. ЗйЩеЗЯОЩЫмСЯПЩНтОіЁААзЩЋЮлШОЁБ
C. КЯРэЪЙгУХЉвЉЃЎПЩМѕЩйХЉвЉЖдХЉВњЦЗКЭЛЗОГЕФЮлШО D.РЌЛјОЗжРрЛиЪеДІРэПЩзЊЛЏЮЊзЪдД
3ЃЎЙцЗЖЕФВйзїЪЧЪЕбщГЩЙІЕФБЃжЄЁЃЯТСаЪЕбщВйзїе§ШЗЕФЪЧ ЃЈ ЃЉ
AЃЎCO2ЕФбщТњ B
ЃЎЪеМЏO2 CЃЎЕЮМгвКЬх DЃЎВтШмвКpH
4ЃЎЛЏбЇгыЮвУЧЕФЩэЬхНЁПЕЯЂЯЂЯрЙиЃЌЯТСагаЙиЫЕЗЈжаЃЌВЛКЯРэЕФЪЧ ЃЈ ЃЉ A.БфжЪЪГЦЗжаГЃКЌгаУЙОњЖОЫиЃЌВЛПЩЪГгУ B.ЯђЛ№ЙјжаМгШыЁАЦЎЯуМСЁБдіМгЦфЯЪУРЖШ C.ПОжЦИтЕуЪБМгШыЬМЫсЧтФЦ
D.ЮЊСЫздМККЭЫћШЫЕФНЁПЕЃЌОмОјбЬВнЃЌдЖРыЖОЦЗ
5 .ЪГЦЗЬэМгМСфхЫсМи(KBrO3)ЛсжТАЉЃЌЦфжафхдЊЫи(Br)ЕФЛЏКЯМлЮЊ ( ) A.+1B.+3C.+5 D.ЮоЗЈШЗЖЈ
6. XЃЌYЃЌZШ§жжГЃМћН№ЪєМАЦфбЮШмвКДцдквдЯТЗДгІЃЌдђШ§жжН№ЪєЕФЛюЖЏадЫГађе§ШЗЕФЪЧЃЈ ЂйX+H2SO4=XSO4+H2Ёќ ЂкY+H2SO4ВЛЗЂЩњЗДгІ ЂлY+2ZNO3=YЃЈNO3ЃЉ2+2ZЃЎ A. YЃОXЃОZ
BЃЎ XЃОZЃОY
CЃЎ XЃОYЃО
Z
DЃЎ ZЃОXЃОY
7ЃЎЯТСазіЗЈВЛРћгкМѕЧсЛЗОГЮлШОЕФЪЧ ЃЈ ЃЉ AЃЎШМЩеЭбСђвдМѕЩйЫсгъЕФВњЩњBЃЎХЉвЉЛЏЗЪЕФКЯРэЪЉгУ
10ЃЎГ§ШЅЯТБэЮяжЪжаКЌгаЕФдгжЪЃЌЫљбЁЪдМСКЭВйзїВЛе§ШЗЃЎЃЎЃЎ
ЕФЪЧ ЃЈ ЃЉ
11ЃЎ(4Зж)ЧыФуДг HЁЂOЁЂCЁЂSЁЂNaЁЂCaжабЁдёЪЪЕБЕФдЊЫизщГЩЗћКЯЯргІвЊЧѓЕФЮяжЪЃЌНЋЦфЛЏбЇЪНЬюдкПеИёжаЁЃ
ЃЈ1ЃЉФмЙЉИјКєЮќЕФЦјЬхЕЅжЪЪЧЃЛЃЈ2вЛжжгаЖОЦјЬхЪЧ ЃЛ ЃЈ3ЃЉеєТјЭЗгУЕФДПМюЪЧЃЛЃЈ4ЃЉгУзїИФСМЫсадЭСШРЕФЪЧЁЃ
12ЃЎ(9Зж)ЧђФЋж§ЬњЪЧЩњЬњЕФвЛжжЃЌЫќОпгагХСМЕФж§дьЁЂЧаЯїМгЙЄКЭФЭФЅадФмЃЌгавЛЖЈЕФЕЏадЃЌЙуЗКгУгкжЦдьЧњжсЁЂГнТжЁЂЛюШћЕШИпМЖж§МўвдМАЖржжЛњаЕСуМўЁЃ
ЃЈ1ЃЉЩњЬњЪєгк ЃЈЬюЁАЕЅжЪЁБЁЂЁАЛЏКЯЮяЁБЁЂЁАКЯН№ЁБжажЎвЛЃЉЁЃ
ЃЈ2ЃЉЩњЬњдкГБЪЊЕФЛЗОГФквзЩњатЃЌЬњатЕФжївЊГЩЗж ЃЈаДЛЏбЇЪНЃЉЃЌЦфжаЬњдЊЫиЕФЛЏКЯМлЪЧЁЃЃЈ3ЃЉЩњЛюжаЮвУЧвЊгУЛЏбЇЗНЗЈГ§ШЅЬњатЕФЗДгІЗНГЬЪНЪЧ
ЃЈ4ЃЉгУЬњжЦШнЦїВЛФмЪЂЗХВЈЖћЖрвКЃЌгУЗНГЬЪННтЪЭдвђЃЈ5ЃЉСЖЬњГЇГЃвдНЙЬПЁЂГрЬњПѓЁЂПеЦјЕШЮЊжївЊдСЯСЖЬњЃЌЧыаДГівЛбѕЛЏЬМгыбѕЛЏЬњдкИпЮТЯТЗДгІЕФЛЏбЇЗНГЬЪНЃКЃЛ 13ЃЎЃЈ5ЗжЃЉЯѕЫсМигыТШЛЏМиЕФШмНтЖШЧњЯпШчЭМ8ЫљЪОЃЌЛиД№ЯТСаЮЪЬтЃК
ЃЉ
Ђйt1ЁцЪБЃЌСНЮяжЪжаШмНтЖШНЯДѓЕФЪЧ ЁЃ
Ек 1 вГ ЙВ 2 вГ
Ђкt2ЁцЪБЃЌСНЮяжЪЕФЕШжЪСПБЅКЭШмвКНЕЮТжСt1ЁцЃЌЮіГіЙЬЬхжЪСПНЯДѓЕФЪЧЕФШмвКЁЃ Ђлt2ЁцЪБЃЌНЋ100gЫЎМгШыЪЂга50gТШЛЏМиЕФЩеБжаЃЌГфЗжШмНтКѓЃЌЕУЕНТШЛЏМиЕФЃЈЬюЁАБЅКЭЁБЛђЁАВЛБЅКЭЁБЃЉШмвКЁЃБЃГжЮТЖШВЛБфЃЌЭљИУЩеБжадйМгШы10gЫЎЃЌГфЗжНСАшКѓЃЌТШЛЏМиШмвКЕФШмжЪЕФжЪСПЗжЪ§ ЃЈЬюЁАБфДѓЁБЁЂЁАВЛБфЁБЛђЁАБфаЁЁБЃЉЁЃ
ЂмгћХфжЦШмжЪЕФжЪСПЗжЪ§ЮЊ20%ЕФЯѕЫсМиШмвКЃЌгІТњзуЕФЮТЖШЗЖЮЇЪЧЁЃ 14. (6Зж)ЯжЖдФГЙЬЬхЛьКЯЮяМјБ№ШчЯТЃЌЧыКЯРэзіГіЭЦЖЯЃК
ЃЈ1ЃЉЮоЩЋТЫвКжавЛЖЈКЌга______ЃЌ(ЬюаДРызгЗћКХ)ШєТЫвКжабєРызгЪЧФЦРызгЃЌЧыаДГіЮоЩЋТЫвКAгыЯѕЫсвјШмвКВњЩњАзЩЋГСЕэЕФЛЏбЇЗНГЬЪНЃК________________________ЁЃ
ЃЈ2ЃЉАзЩЋГСЕэBПЩФмЪЧЃК______ЃЌЧыаДГіBгыЯЁбЮЫсЗДгІЕФЛЏбЇЗНГЬЪНЃК____________________________________ЃЛ
15ЃЎ (9Зж)ЙщФЩгыбнвяЪЧживЊЕФПЦбЇЗНЗЈЃЌвВЪЧГЃгУЕФЛЏбЇбЇЯАЗНЗЈЁЃвдЯТЪЧЮвУЧЪьЯЄЕФЪЕбщЪвжЦШЁЦјЬхЕФЗЂЩњзАжУЁЂЪеМЏзАжУвдМАОЛЛЏзАжУЃЈзАжУЂпжаМюЪЏЛвЮЊЙЬЬхЧтбѕЛЏФЦКЭбѕЛЏИЦЕФЛьКЯЮяЃЉЁЃЧыИљОнЯТСаЪЕбщзАжУЛиД№ЮЪЬт
ЃЈ1ЃЉаДГізАжУЂкжаЕФвЛжжвЧЦїЕФУћГЦ__________ЁЃ
ЃЈ2ЃЉаДГігУзАжУЂйжЦШЁбѕЦјЕФвЛИіЛЏбЇЗНГЬЪН ЃЌ ЃЈ3ЃЉЪЕбщЪвгУЪЏЛвЪЏКЭЯЁбЮЫсжЦШЁЖўбѕЛЏЬМЕФЛЏбЇЗНГЬЪНЮЊЁЃЃЌбЁгУЕФзАжУ
зщКЯЪЧ ЃЈЬюађКХЃЉЁЃШєвЊИЩдяЖўбѕЛЏЬМЦјЬхЃЌгІбЁдёвдЩЯзАжУЂоЁЂЂпжаЕФЃЈЬюађКХЃЉЁЃ
ЃЈ4ЃЉБДБДЭЌбЇЩЯЭјВщзЪСЯЕУжЊЃКЪЕбщЪвжЦШЁМзЭщЦјЬхЪЧгУЙЬЬхДзЫсФЦКЭМюЪЏЛвЙВЭЌМгШШЃЌЯжгћжЦШЁ
МзЭщЃЌгІбЁгУЕФЗЂЩњзАжУЪЧЃЈЬюађКХЃЉ ЁЃШєгУЂрРДЪеМЏМзЭщЃЌЦјЬхгІДгЃЈЬюЁАaЁБЁЂЃЎЃЎЃЎ
ЁАbЁБЃЉЖЫНјШыЪеМЏ ЁЃ
16.(9Зж)ЩњЛюжаЕФЪГЦЗАќзАФкГЃИНДјгавЛаЁАќИЩдяМСЃЈЦфжївЊГЩЗжЮЊЩњЪЏЛвЃЉЃЌПЩаЁУїТђЛиЪГЦЗДђПЊАќзАКѓШДЗЂЯжЪГЦЗФкЕФИЩдяМСНсГЩСЫаЁПщЃЌЖдДЫЫћВњЩњвЩЮЪЃКДЫИЩдяМСЪЧЗёвРШЛЛЙФмЦ№ЕНИЩдязїгУЃПВЂЖдДЫзіГіВТЯыШчЯТЃК
ВТЯывЛЃКДЫИЩдяМСУЛгаБфжЪЃЌШдФмЦ№ЕНИЩдязїгУЁЃ
ВТЯыЖўЃКДЫИЩдяМСБфжЪвбОЪЇаЇЃЛ ВТЯыШ§ЃКДЫИЩдяМСПЩФмВПЗжБфжЪЃЛ ЩшМЦЪЕбщШчЯТБэЫљЪОЃК
гЩДЫаЁУїПЩвдзіГіШчЯТНсТлЃКЪГЦЗАќзАДќФкЕФИЩдяМСВПЗжБфжЪЃЛдкДЫЙ§ГЬжаЩњЪЏЛвБфжЪгыПеЦјжаЕФЫЎКЭ гаЙиЃЌаДГіЗДгІдРэЃЈгУЛЏбЇЗНГЬЪНБэЪОЃЉ ЂйЃЛ Ђк
ЁЃ
ЫФЁЂМЦЫуЬт
17.(3Зж)ЕиЙЕгЭжаКЌгавЛжжЧПСвжТАЉЮяжЪЛЦЧњУЙЫиB2ЃЌЦфЛЏбЇЪНЮЊЃКC17H14O6ЃЌГЄЦкЪГгУЛсв§Ц№ЯћЛЏЕРАЉБфЃЌЧыЛиД№ЃК
ЃЈ1ЃЉЛЦЧњУЙЫиB2жаЬМЁЂЧтЁЂбѕШ§жждЊЫиЕФдзгИіЪ§БШЮЊ ЃЛ ЃЈ2ЃЉЛЦЧњУЙЫиB2ЕФЯрЖдЗжзгжЪСПЮЊ ЃЛ ЃЈ3ЃЉ15.7gЛЦЧњУЙЫиB2жаКЌга gбѕдЊЫиЁЃ
18.(5Зж) НЋ50gТШЛЏИЦШмвКгы77gЬМЫсФЦШмвКЛьКЯКѓЃЌЧЁКУЭъШЋЗДгІЃЌЙ§ТЫЁЂЯДЕгЁЂКцИЩКѓЃЌЕУЕН10gАзЩЋЙЬЬхЁЃЧыМЦЫу(аДГіМЦЫуЙ§ГЬ)ЃК(1)ИУ50gТШЛЏИЦШмвКжаШмжЪЕФжЪСП;(2)Й§ТЫКѓЫљЕУШмвКжаШмжЪЕФжЪСПЗжЪ§ЁЃ
Ек 2 вГ ЙВ 2 вГ
ЯрЙиШШДЪЫбЫїЃК

